Yapıyı Keşfedin
Dendritik hücrenin moleküler donanımını incelemek için soldaki
numaralı noktalara tıklayın.
01
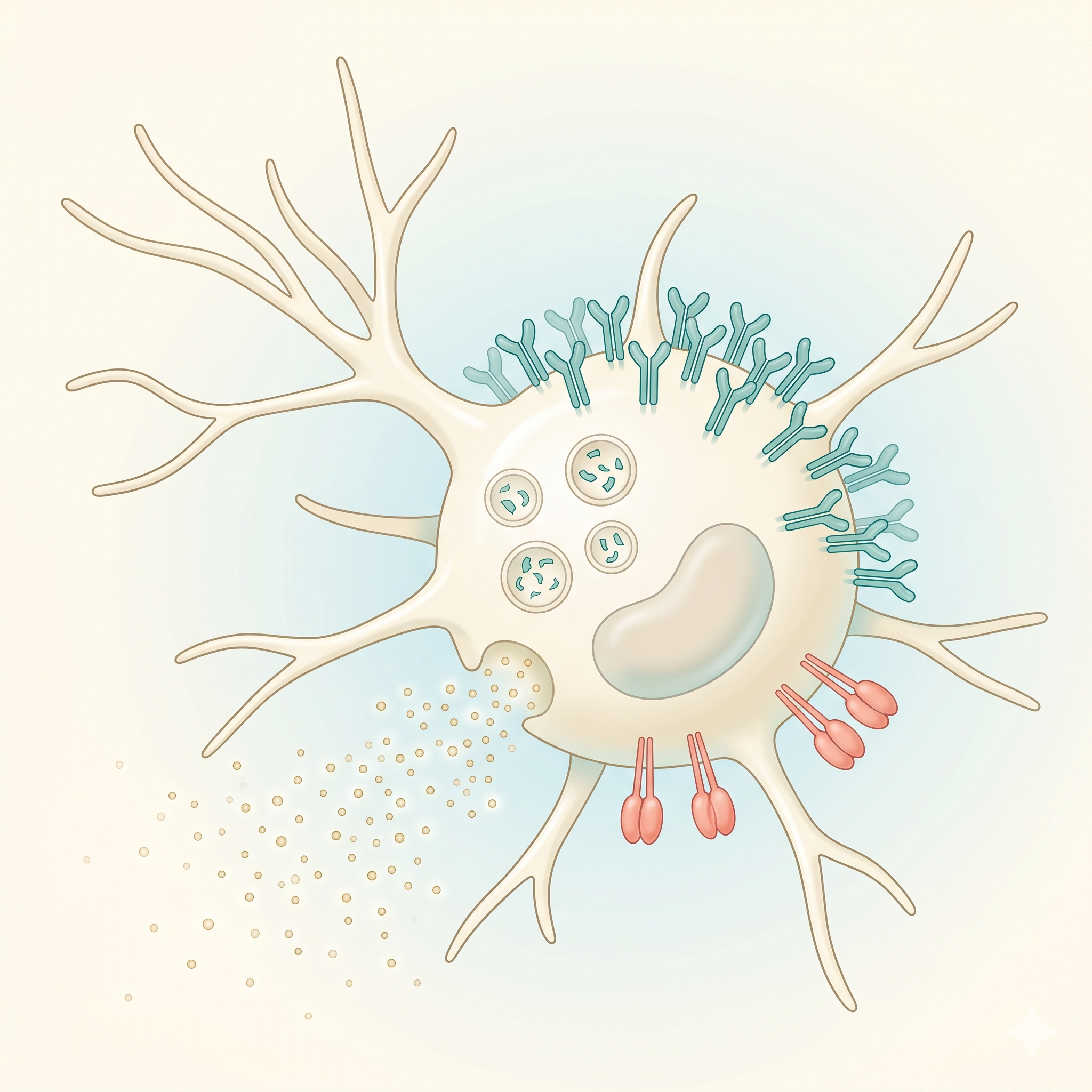
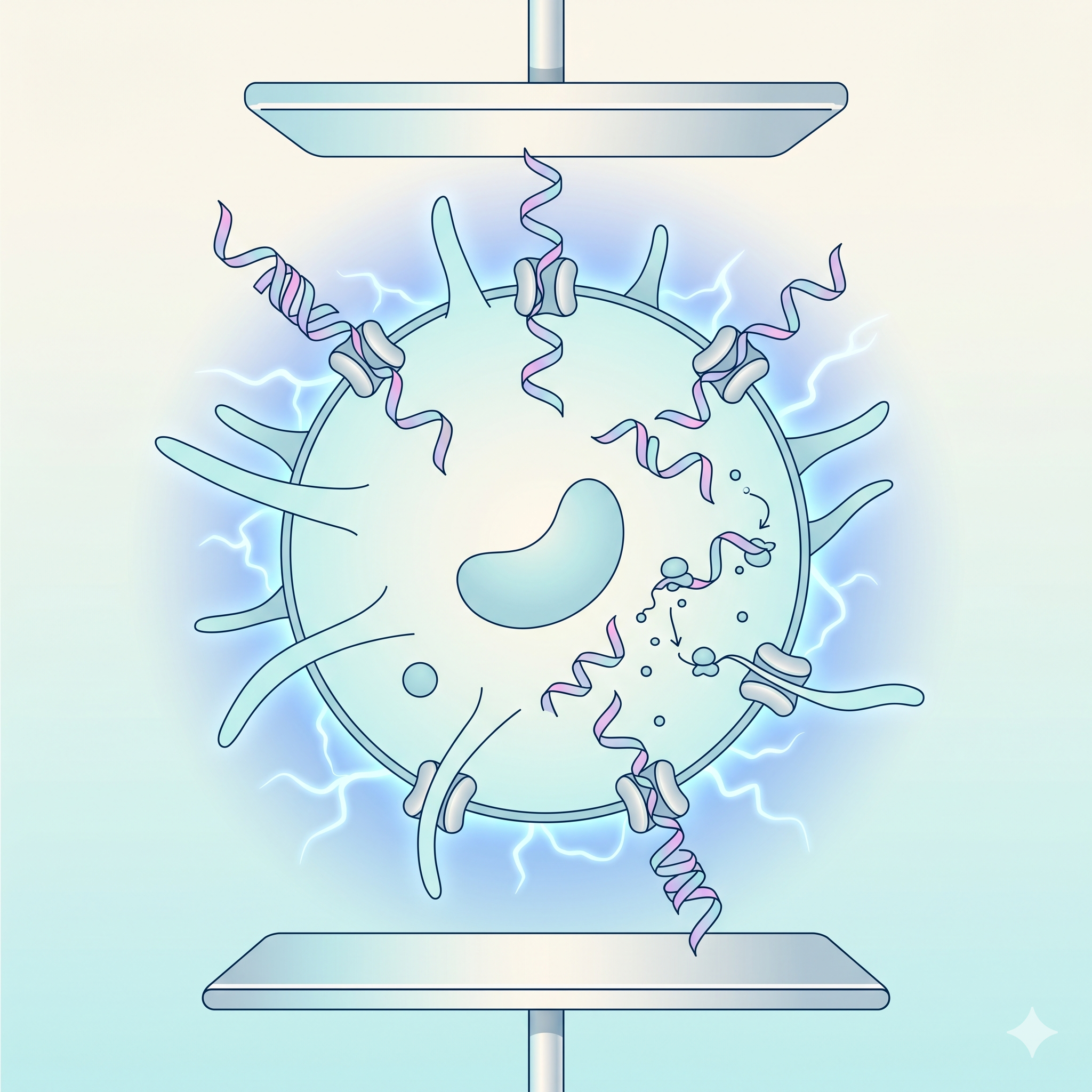
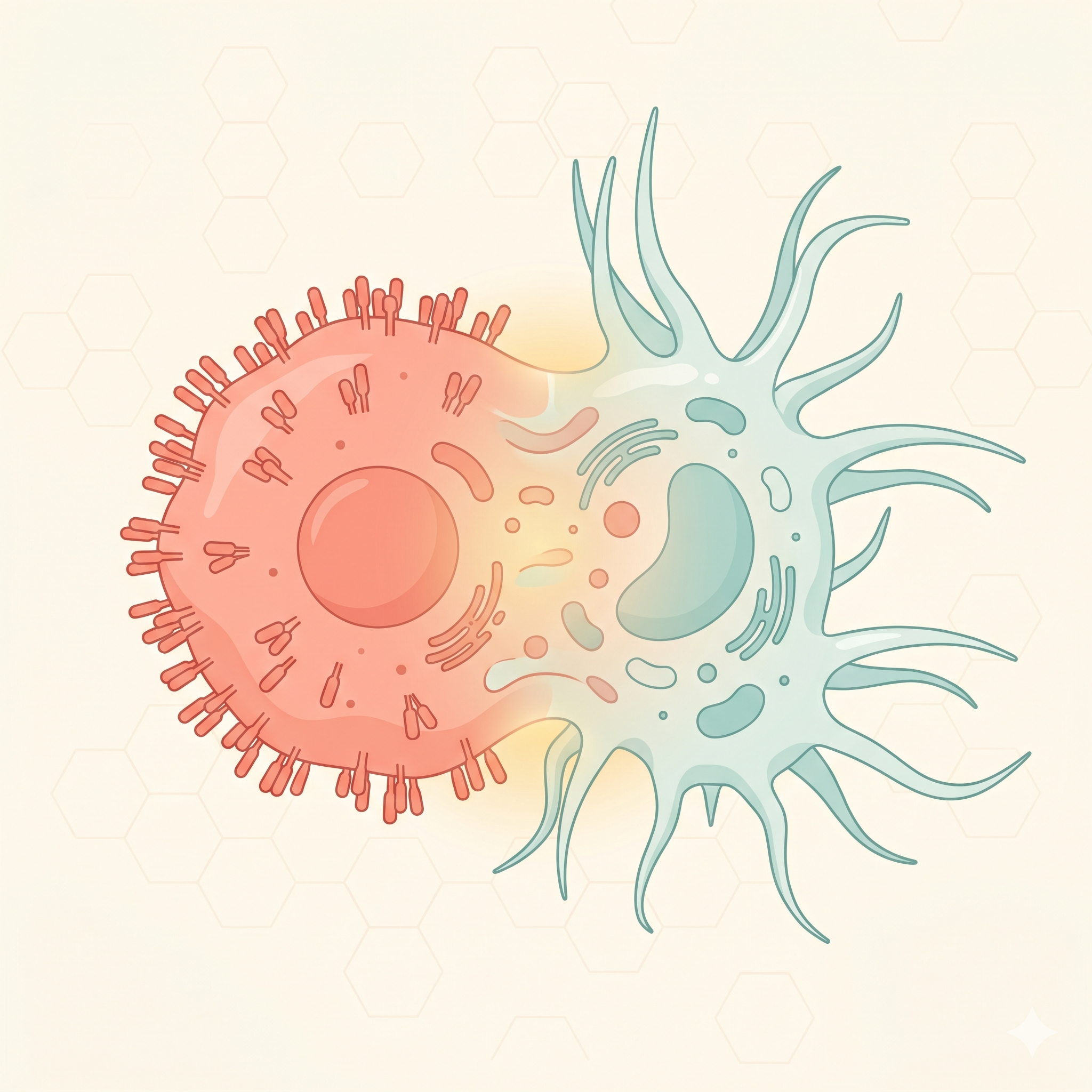
Dendritler
Yıldız şeklindeki uzantılar
Hücreye karakteristik şeklini veren uzun, dallanmış sitoplazmik
uzantılar. Yüzey alanını dramatik şekilde artırarak DC'lerin
antijen yakalama verimliliğini maksimize eder.
Tek bir DC, binlerce T hücresiyle aynı anda etkileşime girebilir.
~10x
küresel hücreden daha geniş yüzey alanı
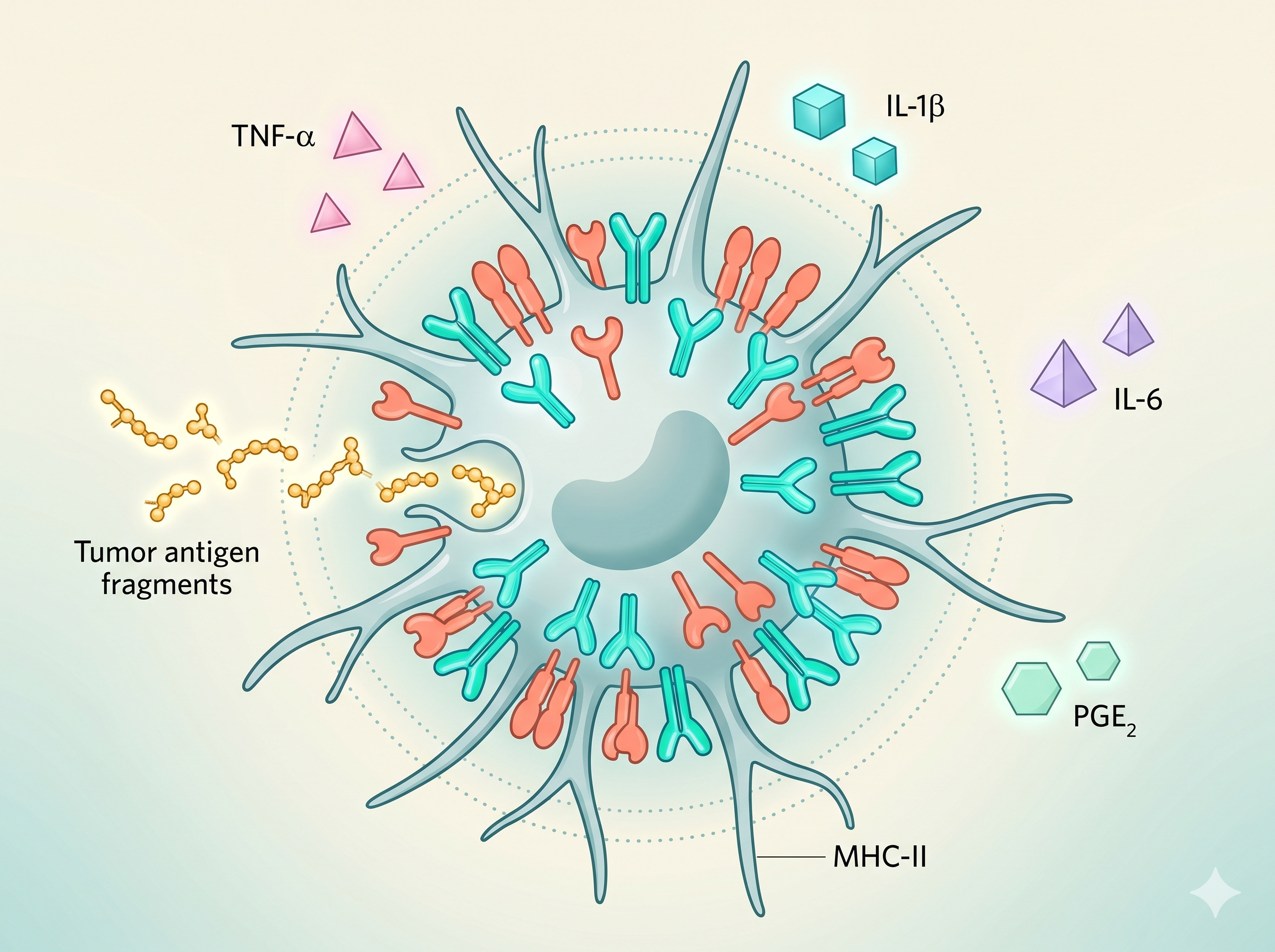
02
MHC-II Molekülleri
HLA-DR, HLA-DP, HLA-DQ
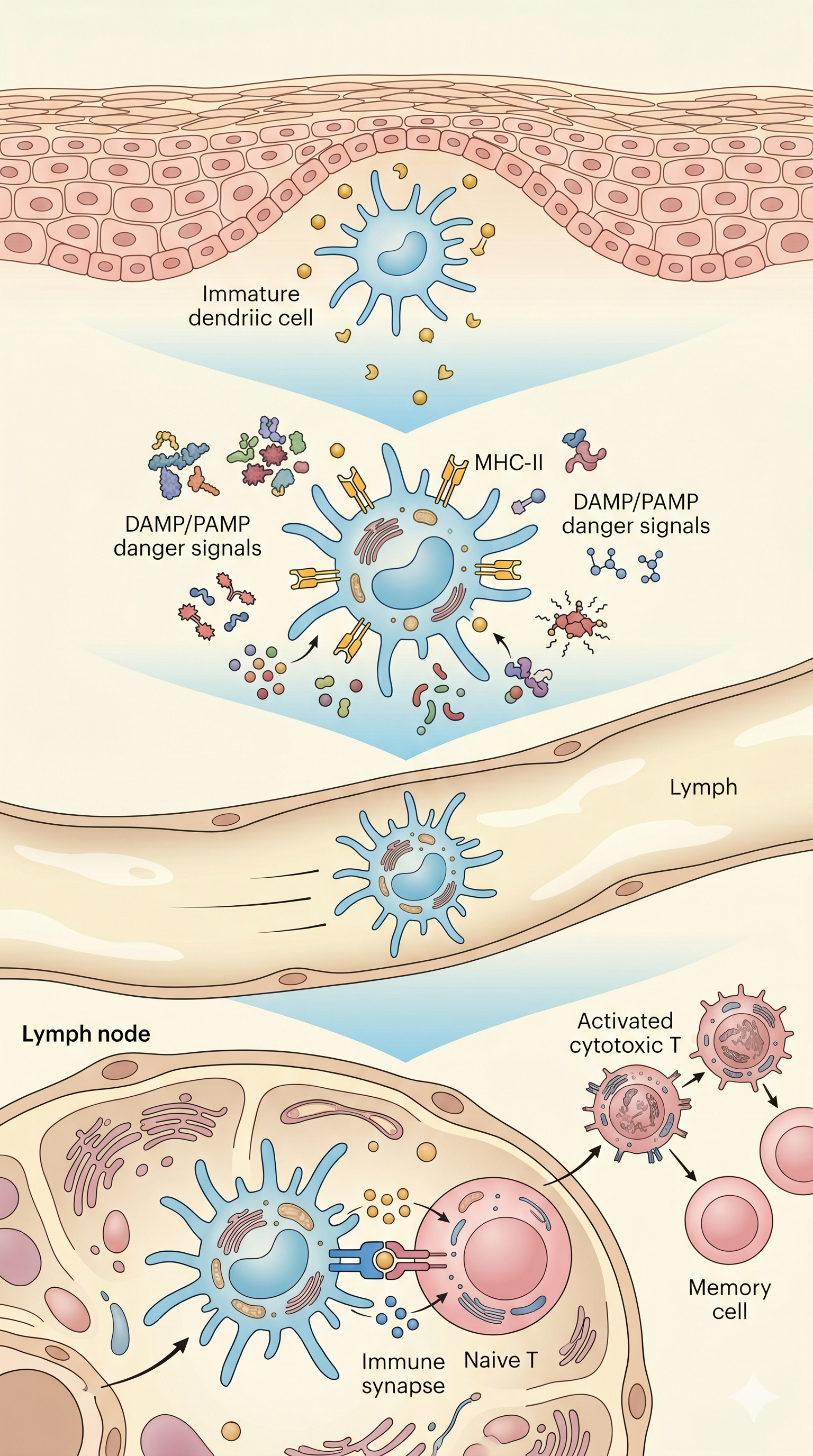
İşlenmiş antijen peptidlerini CD4+ T hücrelerine sunan major
histocompatibility complex sınıf II molekülleri. Olgunlaşan DC'lerde
yüzey ekspresyonu 10-100 kat artar — bu süreç
antijen sunum kapasitesinin imzasıdır.
10⁶+
olgun DC başına yüzey MHC-II molekülü
03
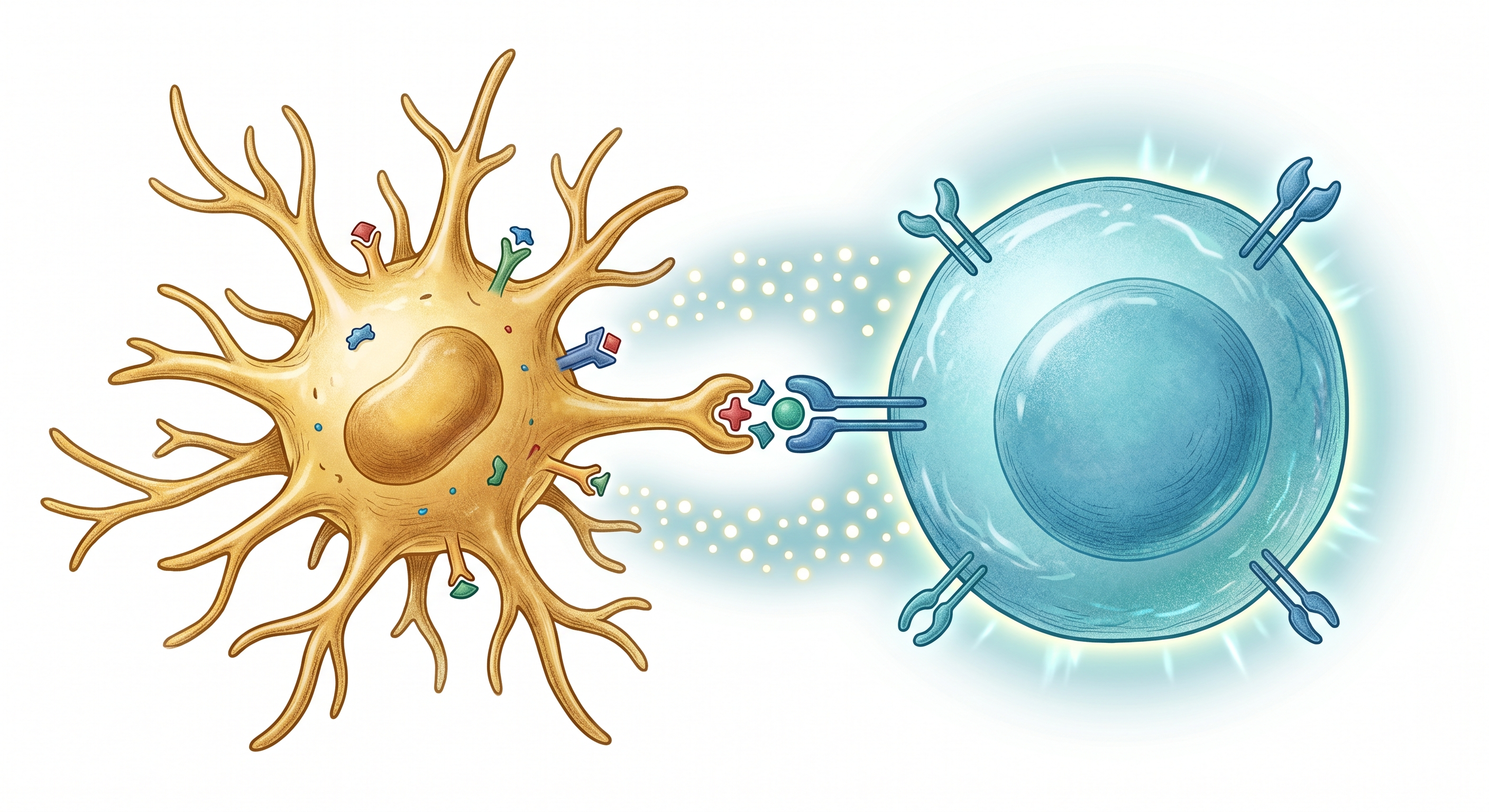
Kostimülatör Moleküller
CD80 (B7-1), CD86 (B7-2), CD40
T hücre aktivasyonu için zorunlu olan "ikinci sinyal"
molekülleri. Bu moleküller olmadan T hücresi anerjiye düşer (tepkisiz
kalır). DC'lerin bu kostimülatör molekülleri yüksek seviyede
sunabilmesi, onları diğer antijen sunan hücrelerden ayıran kritik
özelliktir.
CD28
T hücresindeki kostimülatör reseptör partneri
04
Sitokin Salınımı
IL-12, IL-6, IFN-α, TNF-α
DC'lerin "üçüncü sinyali" — salınan sitokinler T hücrelerinin
farklılaşma yönünü belirler. IL-12 Th1 (anti-tümör)
yanıtı, IL-4 Th2 (humoral) yanıtı yönlendirir. Olgun DC'lerin
anti-tümör sitokin profili, kanser immünoterapisinin temel
mekanizmasını oluşturur.
IL-12
en güçlü Th1 / sitotoksik T hücre indükleyicisi
05
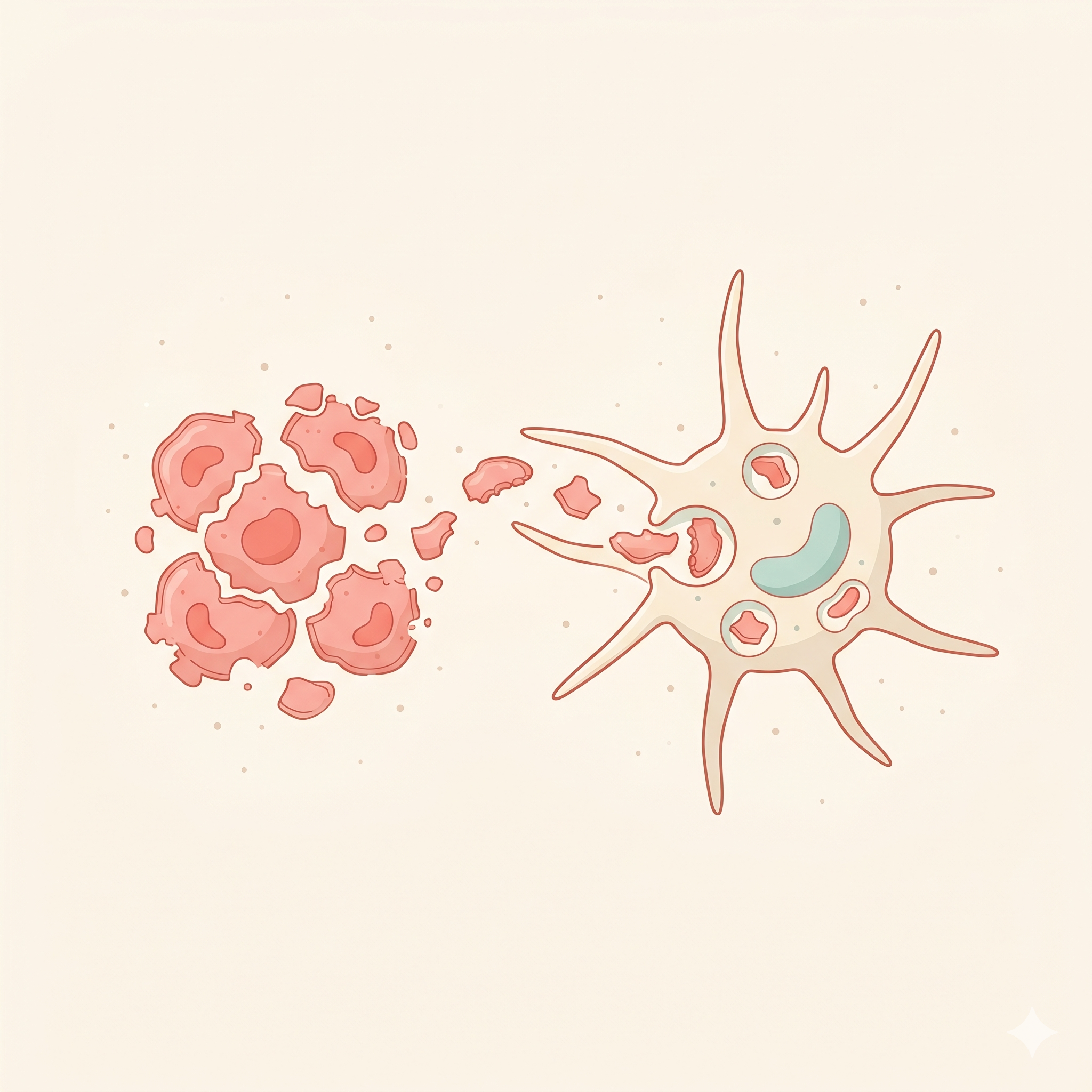
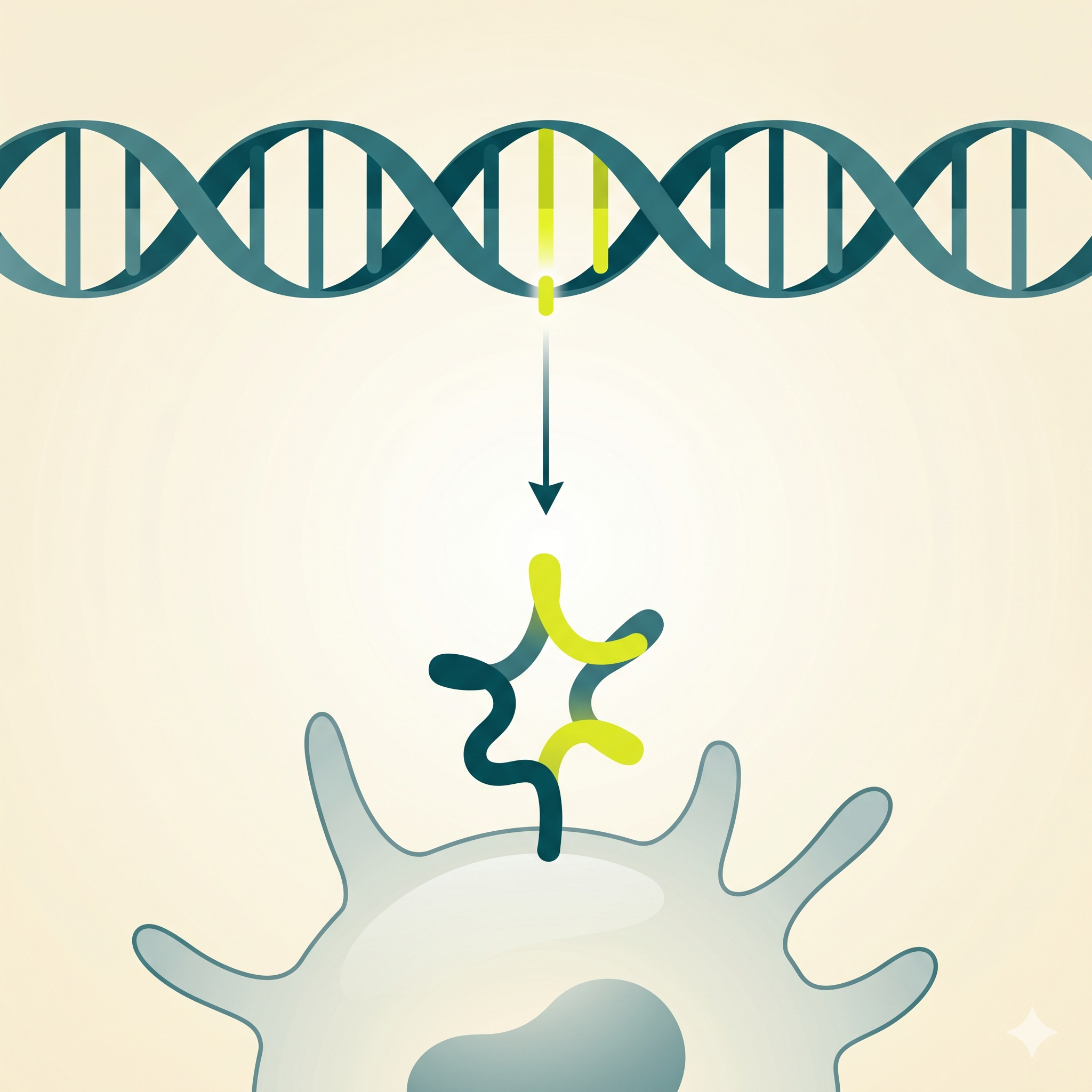
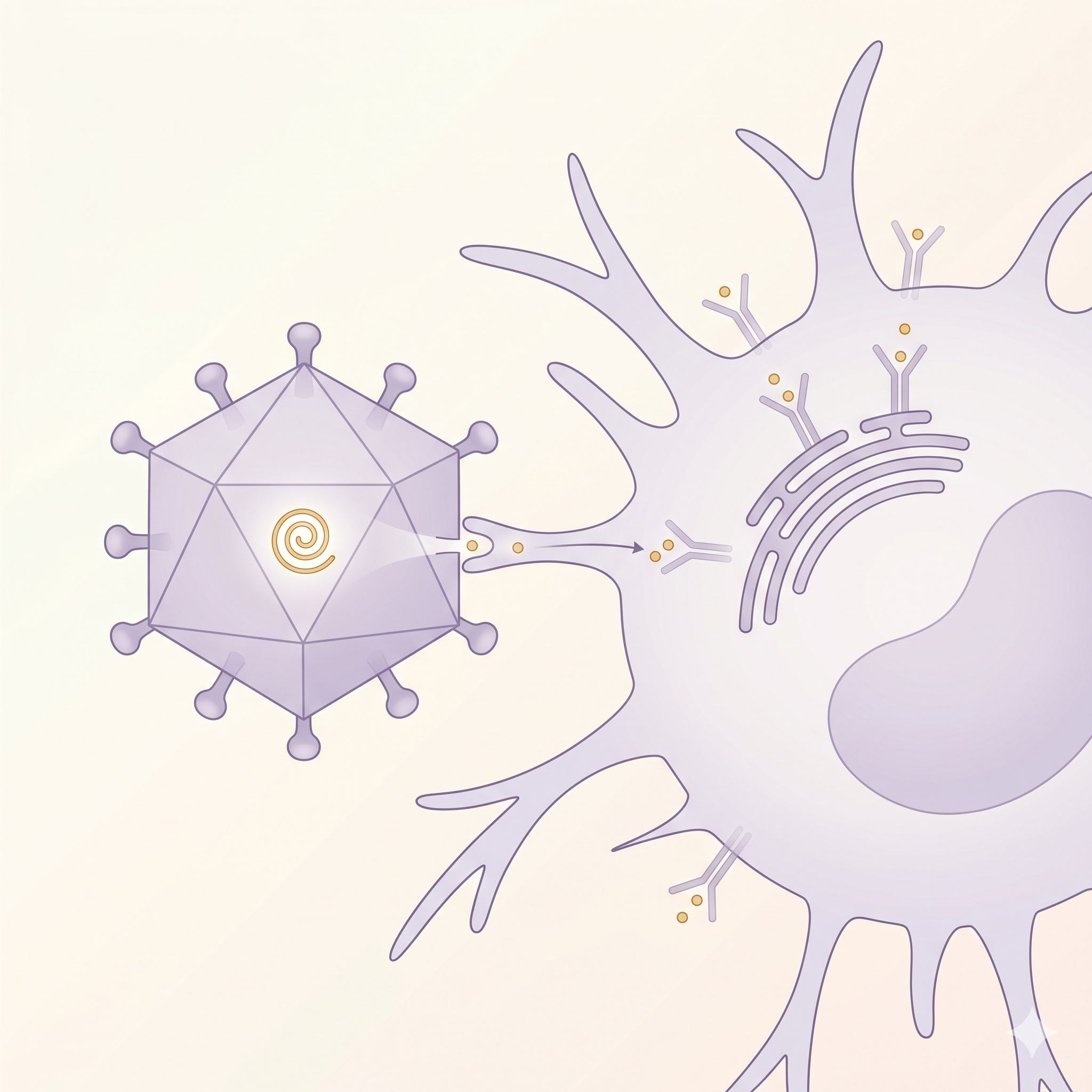
Fagositik Vesiküller
Endozom & fagolizozom
DC'ler ekstrasellüler antijenleri makropinositoz, fagositoz ve reseptör
aracılı endositoz ile yakalar. Bu vesiküllerde antijen peptid
parçalarına ayrıştırılır ve MHC molekülleriyle yüklenir.
DC'lerin çapraz sunum (cross-presentation) yetenekleri
ekstrasellüler antijenleri MHC-I üzerinden CD8+ T hücrelerine
sunmasına olanak tanır — anti-tümör bağışıklığı için kritik.
~24sa
antijen yüklenmesinden olgun sunuma kadar