CD3+CD56+ Efektörler
Ana Efektör
CIK'ın ana saldırı gücü. NKG2D ve DNAM-1 reseptörleri ile MHC-bağımsız sitotoksisite gösterir. Çift yolak (perforin/granzim + Fas/FasL) ile tümör hücrelerini yok eder.
NK hücrelerinin MHC-bağımsız hedef tanıma kapasitesini, T hücrelerinin adaptif yanıt yeteneğiyle birleştiren hibrit immün efektörler.
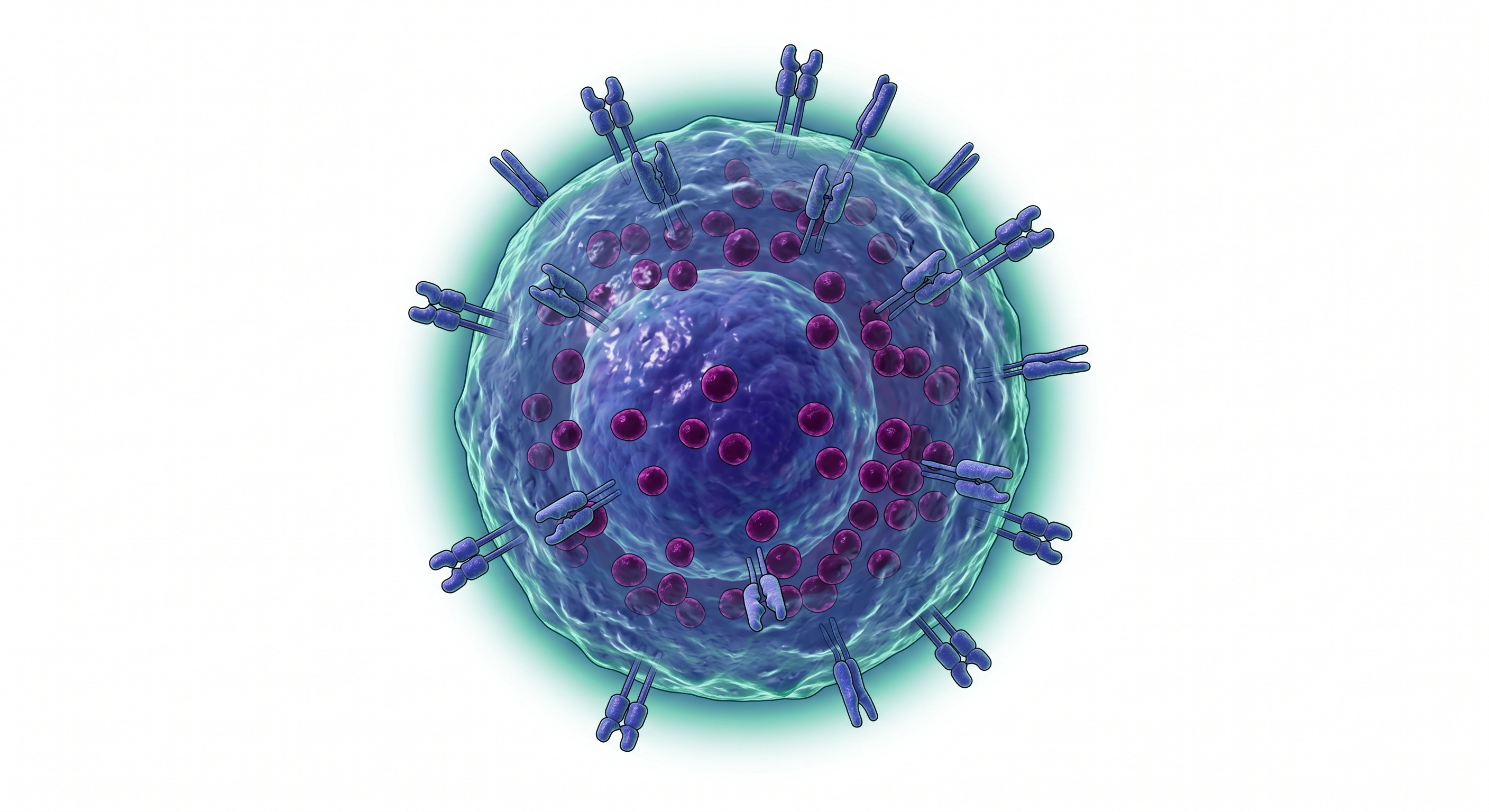
CIK Hücrelerini Keşfet ↓CIK (Cytokine-Induced Killer) hücreleri, periferik kandan izole edilen bağışıklık hücrelerinin IFN-γ, anti-CD3 antikoru ve IL-2 ile ex vivo ortamda aktive edilmesiyle oluşturulan heterojen bir efektör hücre popülasyonudur. CD3+CD56+ çift pozitif fenotipleri sayesinde hem doğal hem edinsel bağışıklığın silahlarını tek bünyede taşır.
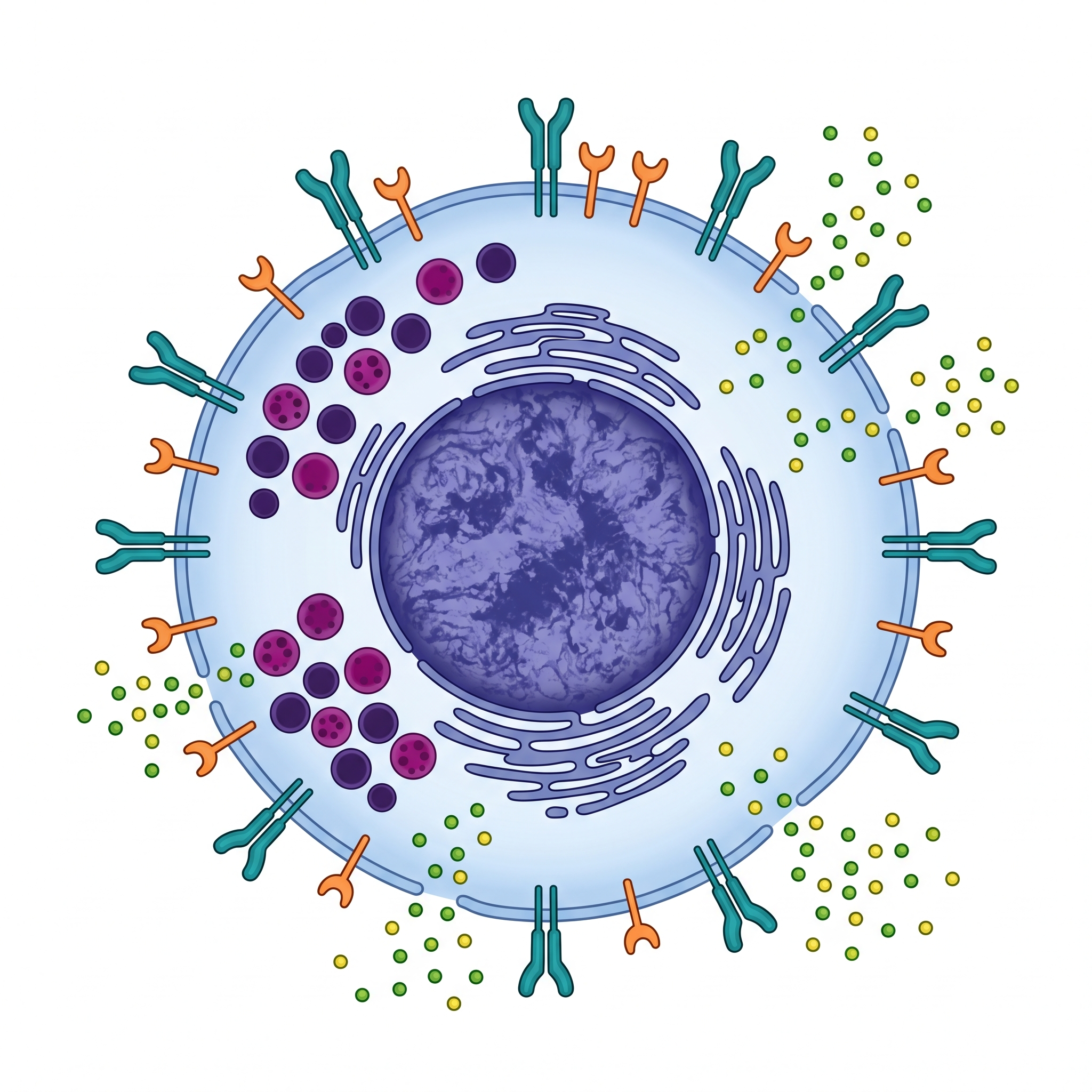
CIK hücresinin farklı bölgelerini incelemek için soldaki numaralı noktalara tıklayın.
Hibrit Yüzey Belirteçleri
CIK hücrelerinin ana efektör popülasyonu, hem T hücre belirteci olan CD3'ü hem de NK hücre belirteci olan CD56'yı birlikte taşır. Bu çift pozitif fenotip, CIK hücrelerine benzersiz bir "NKT-benzeri" karakter kazandırarak iki bağışıklık kolunun avantajlarını birleştirir.
MHC-Bağımsız Tanıma
CIK hücrelerinin temel hedef tanıma mekanizması NKG2D reseptörü üzerinden çalışır. Bu reseptör, stres altındaki ve kanserli hücrelerin yüzeyindeki MICA/MICB ve ULBP ligandlarını tanıyarak MHC-bağımsız sitotoksisiteyi tetikler — tümörün antijen sunumunu kapatarak kaçış girişimlerini etkisiz kılar.
Antijene Spesifik Tanıma
CIK hücreleri, CD3 kompleksi ile bağlantılı fonksiyonel bir T hücre reseptörü taşır. Bu sayede NKG2D aracılı doğal tanımanın yanı sıra antijene spesifik adaptif tanıma kapasitesine de sahiptir. Çift yolak, tümör kaçış mekanizmalarına karşı ikili güvence sağlar.
Perforin & Granzim B
CIK hücreleri NK hücreleri gibi yoğun sitotoksik granüller içerir. Perforin hedef hücre zarında porlar açarken, Granzim B bu porlardan girerek kaspaz kaskadını tetikler ve apoptozu başlatır. CIK hücreleri hasarsız ayrılarak birden fazla hedefi seri olarak yok edebilir.
IFN-γ, TNF-α, IL-2
CIK hücreleri güçlü sitokin üreticileridir. Salgıladıkları IFN-γ makrofajları aktive eder, TNF-α tümör damarlanmasını bozar ve tümör mikroçevresini bağışıklık yanıtına duyarlı hale getirir. Bu "sitokin köprüsü" sayesinde adaptif bağışıklığı da devreye sokarak sistemik immün yanıtı organize eder.
CIK kültürü tek tip bir hücre değildir — üç farklı bağışıklık hücre popülasyonundan oluşan koordineli bir ekosistemdir. Bu heterojenitenin kendisi bir avantajdır: tümör, tek bir kaçış stratejisiyle üçünden birden kurtulamaz.
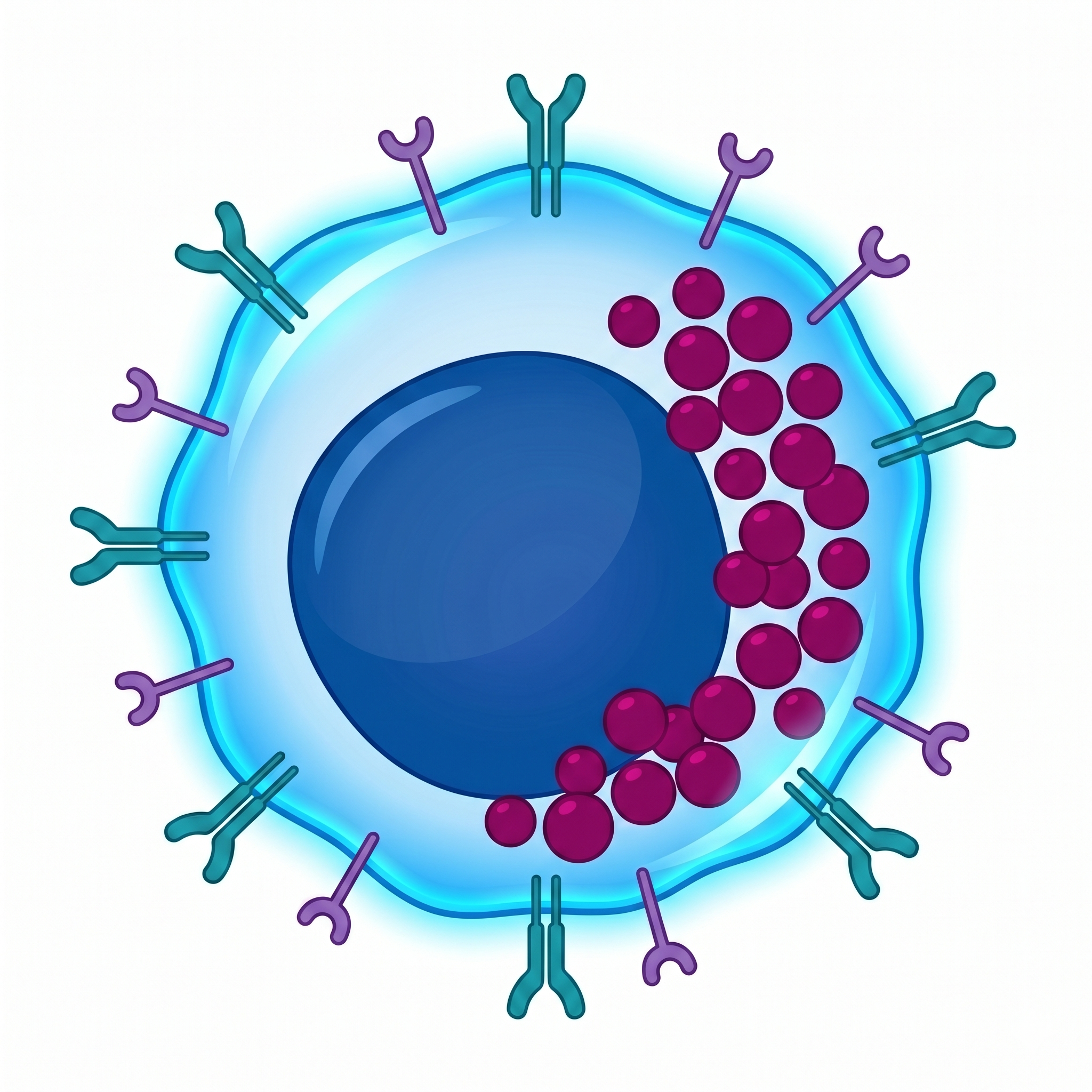 CD3⁺CD56⁺
%20-40
CD3⁺CD56⁺
%20-40
 CD3⁺CD56⁻
%50-60
CD3⁺CD56⁻
%50-60
 CD3⁻CD56⁺
%5-10
CD3⁻CD56⁺
%5-10
Ana Efektör
CIK'ın ana saldırı gücü. NKG2D ve DNAM-1 reseptörleri ile MHC-bağımsız sitotoksisite gösterir. Çift yolak (perforin/granzim + Fas/FasL) ile tümör hücrelerini yok eder.
Adaptif Destek
Kültürün en kalabalık popülasyonu. TCR aracılı antijene spesifik tanıma ve immünolojik hafıza oluşturma yeteneği ile uzun vadeli koruma sağlar.
Doğal Keşif Kolu
Konvansiyonel NK hücreleri olarak ilk temas anında hızlı sitotoksisite sağlar. Sayıca az ama etkisi büyüktür.
CIK tedavisinin en güzel yanlarından biri, üretim sürecinin oldukça basit ve iyi tanımlanmış olmasıdır. Genetik değişiklik gerektirmez — sadece doğru sitokinler ve sabır.
Kültür Başlangıcı
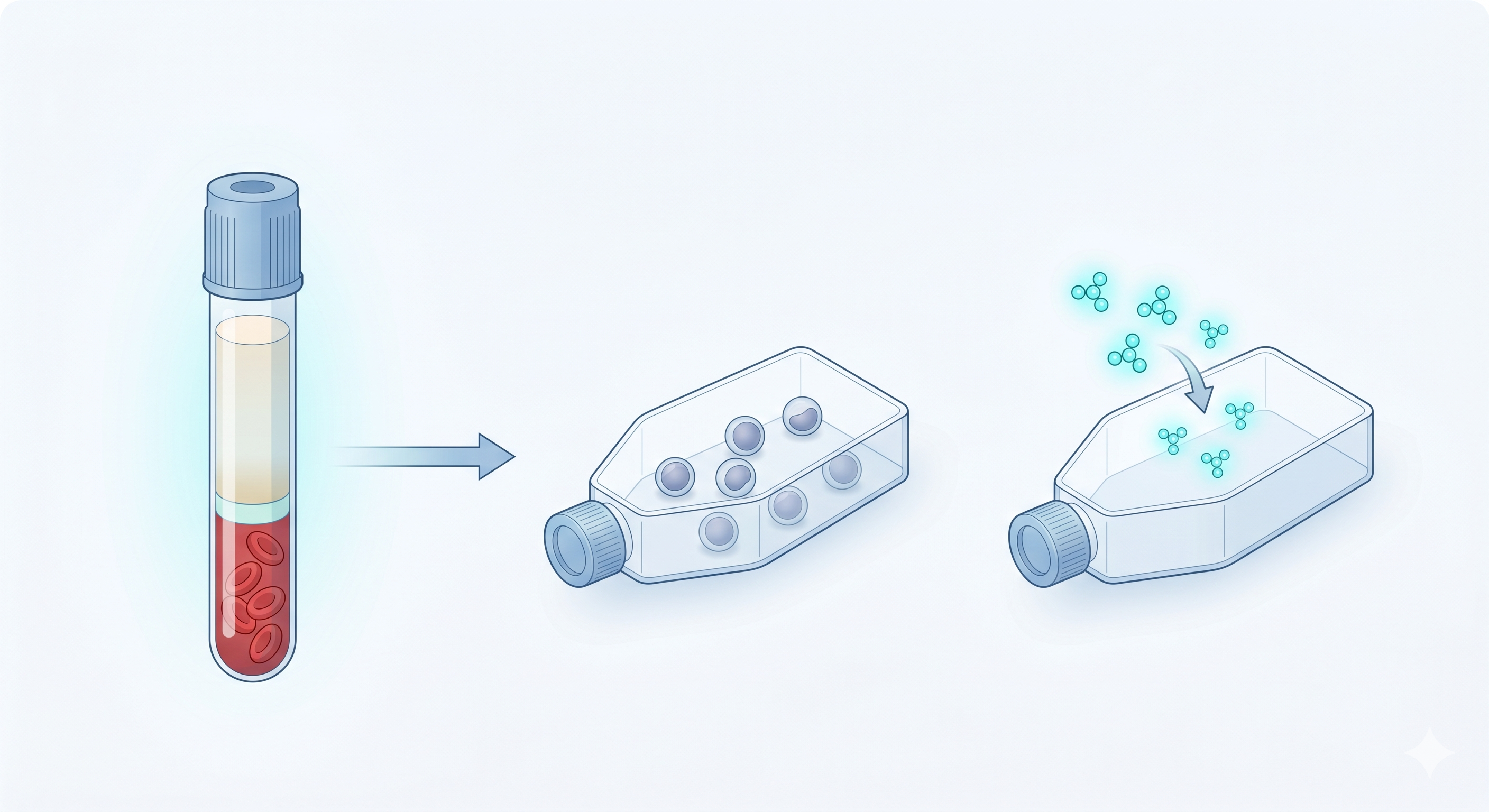
Periferik kandan Ficoll yoğunluk gradiyenti ile mononükleer hücreler (PBMC) izole edilir ve serumsuz kültür ortamına (X-VIVO 15) alınır. İlk adımda 1000 U/mL dozunda IFN-γ eklenir. Bu priming aşaması, hücreleri sonraki mitojenik uyarıya hazırlar ve IL-2 yanıt kapasitesini artırır — 24 saat önceden uygulanması kritik öneme sahiptir.
Hücresel Dönüşüm
İkinci gün iki kritik bileşen eklenir: Anti-CD3 monoklonal antikoru (OKT-3, 50 ng/mL) T hücrelerini aktive ederken, IL-2 (300-600 U/mL) proliferasyonu tetikler. Bu kombinasyon, PBMC'lerin CIK fenotipine dönüşümünü başlatır. Hücreler çoğalmaya ve CD3+CD56+ yüzey ekspresyonu kazanmaya başlar.
Hasat ve Serbest Bırakma
İki ila üç hafta boyunca her 2-3 günde IL-2 ve taze besiyeri eklenerek hücreler ekspanse edilir. Bu süre sonunda başlangıç sayısının yaklaşık 1000 katına ulaşılır. CD3+CD56+ oranı %20-40'a yükselir. Hasat öncesi akım sitometrisi ile fenotip analizi, sterilite testi, endotoksin ölçümü ve canlılık değerlendirmesi yapılır.
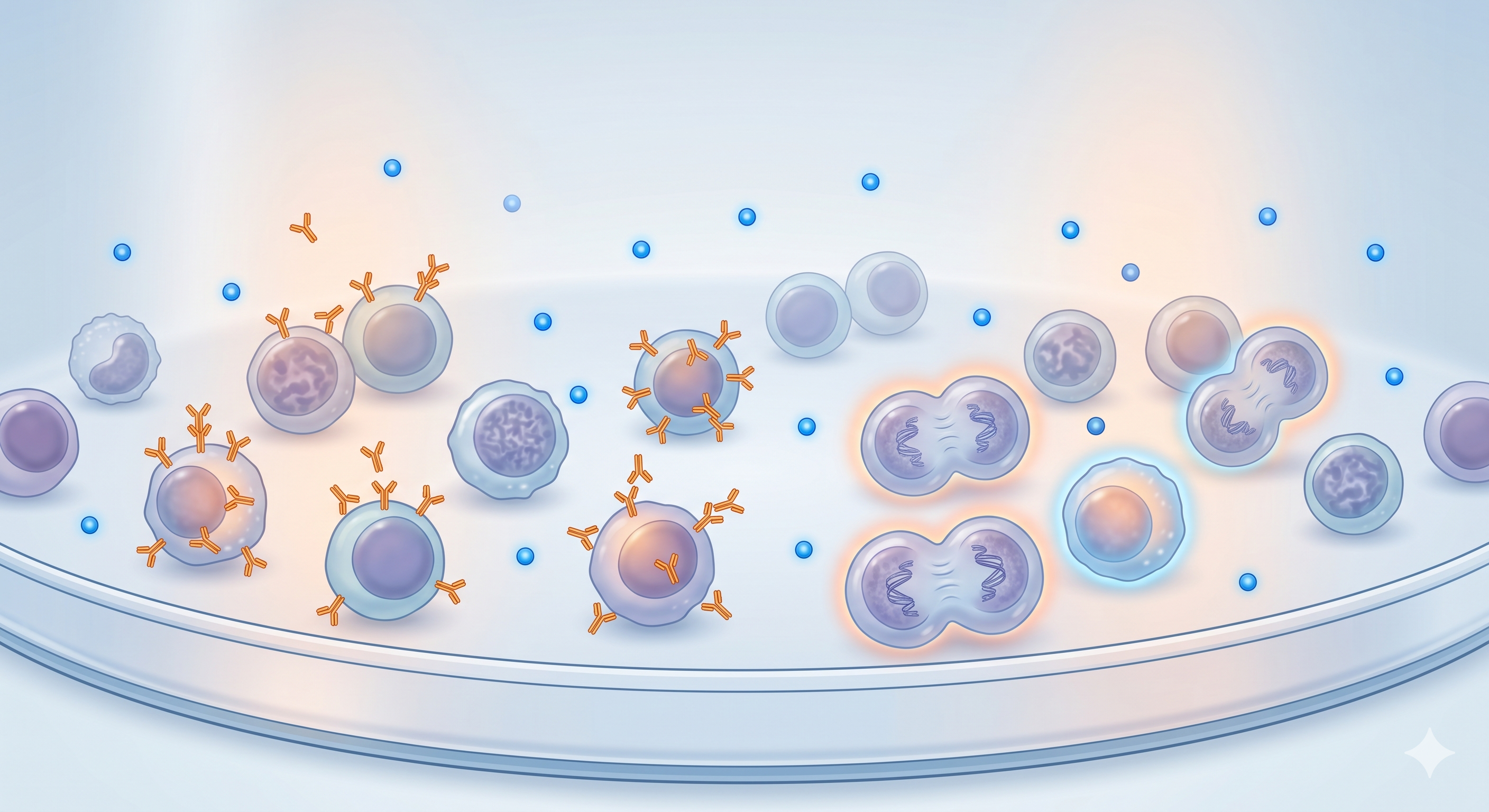

Dünya genelinde 10.000'den fazla hasta üzerinde test edilmiş, klinik çalışmalarla kanıtlanmış sonuçlar.
Karaciğer kanseri (hepatoselüler karsinom, HCC) ameliyat ya da termal ablasyon ile temizlenmiş 230 hasta iki gruba ayrıldı: bir gruba sadece standart takip yapıldı, diğer gruba bunun yanına CIK hücre tedavisi eklendi.
• CIK alan grupta kanserin geri dönme (nüks) riski %38 daha düşük çıktı (Hazard Ratio 0.63; %95 güven aralığı: 0.43-0.94; p=0.010 değeriyle istatistiksel olarak güçlü bir sonuç)
• Nükssüz yaşam süresi de farklıydı: CIK grubunda 44 ay, kontrol grubunda 30 ay
Sonuç: CIK ameliyat ya da ablasyon sonrası verildiğinde, kanserin geri dönmesini ortalama 14 ay geciktiriyor. Karaciğer kanserinde standart bakıma eklenebilecek umut verici bir destek tedavi.
Lee JH, et al., Gastroenterology, 2015; 148:1383-1391Uluslararası CIK Hücre Kayıt Çalışması (IRCC), dünya genelinde yürütülen tüm CIK çalışmalarının toplandığı resmi veri tabanı. 10 yıllık tarama şunu gösteriyor:
• 106 klinik çalışma kayıt altında
• Toplamda 10.225 hasta takip edilmiş
• Bu hastaların 4.889'u doğrudan CIK hücreleriyle tedavi edilmiş
• 30'dan fazla farklı kanser türü hedef alınmış
Sonuç: CIK küçük çaplı, deneysel bir yöntem değil. On binlerce hastayı kapsayan kanıt tabanı sayesinde dünyanın farklı merkezlerinde standartlaşmış bir hücre tedavisi olarak konumlanıyor.
Zhang Y, Schmidt-Wolf IGH, J Cell Physiol, 2020CIK hücreleri bugüne kadar 30'dan fazla farklı kanser türünde test edildi. En güçlü klinik kanıtlar şu kanser tiplerinde elde edilmiş:
• Karaciğer kanseri (hepatoselüler karsinom, HCC)
• Kalın bağırsak kanseri (kolorektal)
• Böbrek kanseri (renal hücreli karsinom)
• Akciğer kanseri (NSCLC)
70 ayrı çalışmayı ve 6.743 kalın bağırsak kanseri hastasını kapsayan büyük bir meta-analizde, CIK alan hastalarda genel sağkalımın Hazard Ratio'su 0.59, hastalıksız sağkalımınki ise 0.55 olarak çıktı.
Sonuç: CIK iki immün hücrenin (NK ve T hücresi) özelliklerini bir araya getirir. Standart tedaviye eklendiğinde ölüm riskinde %41 azalma görülüyor. Birçok kanser türünde işe yarayabileceğini gösteriyor.
Li CMY, et al., J Immunother Cancer, 2023CIK üretimi şöyle işliyor: hastadan alınan kanın içindeki bağışıklık hücreleri, laboratuvarda özel sitokinlerle (IL-2, IFN-γ, anti-CD3 antikoru) uyarılıyor.
• Toplam üretim süresi 14-21 gün
• Bu sürede hücreler yüzlerce ila 1.000 kat çoğalıyor
• CAR-T'nin aksine genetik mühendislik gerekmiyor
Sonuç: CIK, yaklaşık 3 hafta içinde uluslararası ilaç üretim standartlarında (cGMP) hazırlanabiliyor. CAR-T'ye göre hem çok daha basit hem de çok daha uygun maliyetli. Bu da tedaviye erişimi hızlandıran en önemli faktörlerden biri.
Sharma P, Schmidt-Wolf IGH, J Exp Clin Cancer Res, 2021; 40:341Detaylar için kartlara tıklayın
20 yılı aşkın klinik deneyim, CIK hücre tedavisinin üstün güvenlik profilini ortaya koymuştur. Meta-analizler, CIK tedavisinin standart tedaviye kıyasla ciddi yan etkileri artırmadığını göstermektedir.
CAR-T tedavisinde sık görülen ciddi sitokin salınım sendromu (CRS), CIK hücrelerinde son derece nadir ve hafif seyirlidir. Kontrollü immün yanıt oluşturur.
Merkezi sinir sistemi üzerinde olumsuz etki raporlanmamıştır. CIK hücreleri hedef dışı nörolojik hasar oluşturmaz.
CIK hücreleri NKG2D aracılı hedef tanıma sayesinde sağlıklı dokuları korur. Allojenik kullanımda dahi GvHD oranı düşüktür.
Genetik modifikasyon veya viral vektör gerektirmez. Standart GMP koşullarında sitokin kokteyli ile 14-21 günde üretilir. CAR-T'ye kıyasla maliyet-etkin.
NKG2D reseptörünün geniş ligand tanıma kapasitesi sayesinde 30'dan fazla farklı kanser türüne karşı anti-tümör aktivite gösterir.
CIK hücreleri iki farklı yoldan saldırır: granül salınımı (perforin) ve ölüm sinyali (Fas/FasL). Bir yol kapansa diğeri devreye girer.
Lee et al., Gastroenterology 2015 • Zhang & Schmidt-Wolf, J Cell Physiol 2020 • Sharma & Schmidt-Wolf, J Exp Clin Cancer Res 2021
Dendritik hücreler (DC) tümör antijenlerini işleyerek CIK hücrelerine sunar. Bu çift yönlü etkileşim, her iki tedavi modalitesinin tek başına sağlayamayacağı güçlü bir anti-tümör yanıt oluşturur.
Tümör-ilişkili antijenleri toplar, işler ve MHC molekülleri üzerinden sunum için hazırlar.
DC, işlenmiş tümör antijenlerini CIK hücrelerine sunar. Çift yönlü etkileşim IL-12 salınımını artırarak sitotoksisiteyi güçlendirir.
Antijen bilgisiyle donatılmış CIK hücreleri, NKG2D ve TCR aracılı çift yolakla hedefe yönelik sitotoksisiteyi artırır.
Lin et al., Immunol Lett 2017 • Jiang et al., J Transl Med 2024
Genkord, hem DC hem CIK hücrelerini kendi cGMP sertifikalı laboratuvarında üreten nadir altyapılardan biridir.
CIK hücrelerini kendi AR-GE laboratuvarımızda, uluslararası standartlarda geliştiriyor ve üretiyoruz. Yerli üretim, global kalite.

CIK hücrelerini dış kaynaklara bağımlı olmadan, kendi GMP uyumlu AR-GE tesislerimizde geliştiriyoruz.
Kan alımından CIK hasadına, kalite kontrolden klinik uygulamaya tüm süreçler tek çatı altında yönetilir.
GMP standartlarına uygun süreçler, uluslararası sertifikasyonlar ve sürekli denetim altyapısı.
NK, CIK ve Dendritik Hücre — üç farklı hücresel terapi platformunu aynı laboratuvarda üretebilen nadir altyapılardan biri.
CIK (Cytokine-Induced Killer) hücreleri, hastanın veya sağlıklı bir donörün periferik kanından izole edilen mononükleer hücrelerin laboratuvar ortamında IFN-γ, anti-CD3 antikoru ve IL-2 sitokinleri ile aktive edilmesiyle üretilir. 14-21 günlük kültür sürecinde hücreler yaklaşık 1000 kat çoğalır ve güçlü anti-tümör aktivite kazanır. Genetik modifikasyon gerektirmediği için üretim süreci CAR-T'ye kıyasla çok daha basit ve maliyet-etkindir.
NK hücreleri yalnızca doğal bağışıklık mekanizmalarını kullanırken, CIK hücreleri hem NK hem T hücre özelliklerini birleştirir. CIK'ın ana efektör popülasyonu olan CD3+CD56+ hücreler, NKG2D reseptörü ile MHC-bağımsız tanıma yapar (NK-benzeri), aynı zamanda TCR üzerinden antijene spesifik yanıt verebilir (T-benzeri). Bu çift mekanizma, tek yolağa dirençli tümörlere karşı avantaj sağlar.
Evet. 20 yılı aşkın klinik deneyim, CIK hücre tedavisinin üstün güvenlik profilini kanıtlamıştır. En sık görülen yan etkiler hafif ateş (Grade 1-2) ve geçici yorgunluktur. CAR-T tedavisinde sık görülen ciddi sitokin salınım sendromu (CRS), nörotoksisite ve şiddetli GvHD riskleri CIK tedavisinde son derece düşüktür. Meta-analizler, ciddi advers olay oranının %5'in altında olduğunu göstermektedir.
CIK hücre tedavisi 30'dan fazla farklı kanser türünde araştırılmıştır. En güçlü kanıt tabanı hepatoselüler karsinom (HCC), kolorektal kanser, renal hücreli karsinom ve NSCLC'dedir. Randomize kontrollü çalışmalarda özellikle cerrahi veya kemoterapi sonrası adjuvan olarak kullanıldığında nükssüz sağkalımı anlamlı ölçüde iyileştirdiği gösterilmiştir.
DC-CIK, Dendritik Hücre (DC) ve CIK hücrelerinin birlikte kullanıldığı bir kombinasyon tedavisidir. Dendritik hücreler tümör antijenlerini işleyerek CIK hücrelerine sunar — bu antijen sunumu sayesinde CIK hücreleri hedefe yönelik daha spesifik ve güçlü bir sitotoksik yanıt oluşturur. Klinik çalışmalarda DC-CIK kombinasyonunun tek başına CIK tedavisine göre daha yüksek yanıt oranları sağladığı gösterilmiştir. Genkord, hem DC hem CIK'ı aynı laboratuvarda üretebilmektedir.
CAR-T tedavisi viral vektör aracılı genetik modifikasyon, kişiye özel üretim süreci ve haftalarca süren karmaşık bir protokol gerektirir — ABD'de tedavi başına maliyet 300.000 doları aşabilir. CIK hücrelerinde ise genetik modifikasyon yoktur: GMP ortamında yalnızca klinik sınıf sitokinlerle (IFN-γ, IL-2, anti-CD3) 14-21 günde üretilir. Bu standartlaştırılmış ve basit protokol, üretim maliyetini önemli ölçüde düşürür ve erişilebilirliği artırır.
CIK hücre tedavileri, DC-CIK kombinasyonu, AR-GE iş birlikleri veya klinik çalışma ortaklıkları hakkında ekibimizle iletişime geçin.